紫外線フィルターとしての生物鉱化外殻: Biomineral Outer Shell as an UV Filter
Cyrtoidea” from Ernst Haeckel’s Kunstformen der Natur, 1904
多くの生物は鉱化外殻を持つ。現生の生物では、円石藻、有孔虫(炭酸カルシウム)、珪藻、放散虫(シリカ)などの植物プランクトンが美しい外殻を持っている。また、サンゴ類(炭酸カルシウム)や海綿類(シリカと炭酸カルシウム)の外殻を作っている。光合成をする水生生物に外殻を持つものが多いように思われる。
水中に豊富にある重炭酸イオン(HCO3-)の利用が、必然的に炭酸塩の析出を促すことはすでに論じた。しかし、シリカの外殻を持つ珪藻や放散虫の場合は、この論理は成立しそうにない。
そこで、鉱化外殻が紫外線フィルター機能を持っていると考えた。光合成に利用する700nm付近の赤い光を透過し、紫外線を反射するフィルターを持つメリットは光合成生物にとって大きい。光合成をするためには、強い日射に耐えなければならないが、太陽光の中で紫外線(波長400nm以下)は、有害である。植物プランクトンは多くの紫外線吸収物質を生産しているが、それだけですべての紫外線を彼らの体長の範囲で防ぐのは難しい。また、これらの生合成のコストは、光合成に必要な色素の合成と同程度のエネルギーを要し、紫外線が強い場合には、主要な増殖制約要因となっている(Dillon et al. 2002; Liu et a., 2004; Shinha and Haeder 2002)。
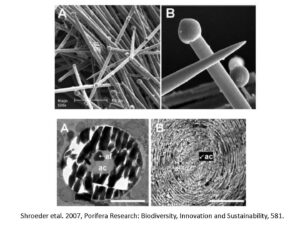
植物プランクトンやサンゴが作る鉱物の特徴は、サブミクロンサイズの小さな粒子が結合してできていることである。このような微小な粒子による光の散乱は、ミーの理論により計算され、波長と粒径と形状の複雑な関数で表される。形状が球形の場合その散乱断面積は、波長が粒径より短いときにはその粒子の断面積に一致し、波長が粒径より長くなるにつれて、緩やかに振動しつつ、波長の逆数におおむね比例して減少していく。したがって、外殻がサブミクロンサイズ(粒径300nm-500nm)の粒子の集合体とみなせる場合には、波長350nmの紫外線の散乱断面積は、波長700nmの赤い光に対して、倍近くになる。このような粒子でできた構造が1ミクロン(粒径の数倍)程度あれば、紫外線フィルターとして機能する。ここに、紫外線を強く吸収する色素や金属塩が混ざるとその効果は倍加する。実際、Phenix et al. (2001)は、アイスランドの温泉に生息する現生のストロマトライトコロニーを調査し、鉄シリカ鉱物のバイオフィルム(150-250ミクロン)が、紫外線を可視光に比べて一桁以上強く吸収することを見出した。
紫外線フィルターの機能を発揮するために、サブミクロン粒子がある程度重なって存在することのみが重要であって、その形の詳細にはよらない。このことは、珪藻や円石藻、放散虫の外殻の形が多様であることと調和的である。外殻の形にはそれほど強い選択圧がかかっていないことを意味しているからである。
生物鉱化の遺伝子群は、シアノバクテリアに起源する可能性が高い。最初の酸素発生型光合成生物であるシアノバクテリアは、炭酸塩やシリカの生体鉱化を大いに利用した最初の生物でもあった。始生代、原生代を通して普遍的にみられるストロマトライトは、シアノバクテリアを主体とするコロニーの化石である。ストロマトライトには、炭酸塩を主成分としたものの他にシリカを主成分としたものもみられる(Knoll 2003)。実際、温泉内のケイ酸に富む水中のシアノバクテリアのコロニーでは今もシリカ鉱化が行われている(Kurt et al. 2001)。その鉱化作用はシアノバクテリアコロニーに、外力、捕食者、乾燥とともに、紫外線からの保護を与えている(Phoenix et al. 2001)。
シアノバクテリアが獲得した生物鉱化のための遺伝子群は、真核生物の成立前後に起こった細菌どうしの共生を経て、各種の真核生物に水平伝搬したと考えられる。実際、普通海綿類で、細菌との共生が現在でも観察される。(Unson et al. 1994)。Jackson et al. (2010)は、共生バクテリアが普通海綿類の一種の生物鉱化にかかわっていることを示した。生物鉱化にかかわる遺伝子群の水平伝搬は、このような共生を通して、繰り返しさまざまな種で並行して起こった(Knoll 2003)。
1)Bruemmer F., 2008, Light inside sponge, 2008, Journal of Experimental marine Biology and Ecology, 367, 61-64.
2)Dillon, J.G., Tatsumi, C.M., Tandingan, P.G. and Castenholz, R.W., 2002, Effect of environmental factors on the synthesis of scytonemin, a UVscreening pigment, in a cyanobacterium (Chroococcidiopsis sp.), Arch. Microbiol., 177, 322-331.
3)Jackson, D. J. et al. 2010, An evolutionaly fast-track to biocalcification, Geobiology, 8, 191-196.
4)Knoll, A. 2003, Biominerizatuion and Evolutional History, Rev. Mineral. Geochem. 54, 329-356.
5)Kurt O. et al. 2001, Microbial-silica interactions in Icelandic hot spring sinter: possible analogues for some Precambrian siliceous stromatolites, Sedimentology, 48, 415-433.
6)Phoenix, V.R. et al. 2001, Role of biomineralization as an ultraviolet shield: Implications for Archean life, Geology, 29, 823-829
7)Sinha, R.P. and Haeder, D.-P, Impacts of ultraviolet-B radiation on rice-field cyanobacteria, J. Photosci., 2002, 9, 439-441.
8)Uson, M.D., 1994, A brominated secondary metabolite synthesized by the cyanobacterial symbiot of a marin sponge and accumulation of the crystalline metabolite in sponge tissue, Marine Biology, 119, 1-11.

科学はひとつ 宇宙物理学者による知的挑戦の記録
戎崎俊一 著
学而図書/四六判 並製320頁/本体2,400円+税
12年にわたり「戎崎の科学は一つ」で執筆されてきた記事を精選し、「地震と津波防災」など全9章に再編。すべての章に著者書き下ろしの解説を加えて集成した一冊。